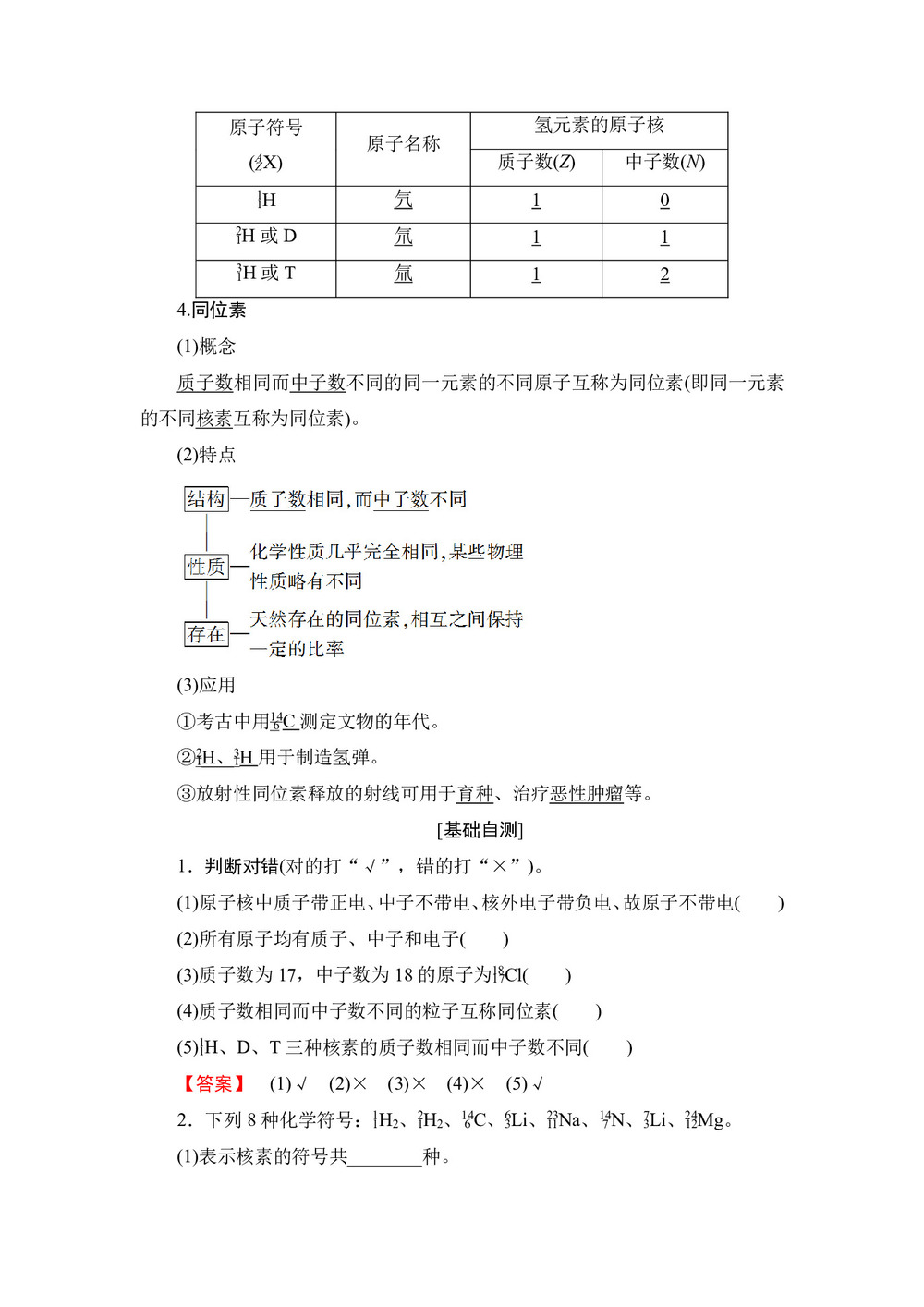
原子符号
(X) 原子名称 氢元素的原子核 质子数(Z) 中子数(N) H 氕 1 0 H或D 氘 1 1 H或T 氚 1 2 4.同位素
(1)概念
质子数相同而中子数不同的同一元素的不同原子互称为同位素(即同一元素的不同核素互称为同位素)。
(2)特点
(3)应用
①考古中用C测定文物的年代。
②H、H用于制造氢弹。
③放射性同位素释放的射线可用于育种、治疗恶性肿瘤等。
[基础自测]
1.判断对错(对的打"√",错的打"×")。
(1)原子核中质子带正电、中子不带电、核外电子带负电、故原子不带电( )
(2)所有原子均有质子、中子和电子( )
(3)质子数为17,中子数为18的原子为Cl( )
(4)质子数相同而中子数不同的粒子互称同位素( )
(5)H、D、T三种核素的质子数相同而中子数不同( )
【答案】 (1)√ (2)× (3)× (4)× (5)√
2.下列8种化学符号:H2、H2、C、Li、Na、N、Li、Mg。
(1)表示核素的符号共________种。
(2)互为同位素的是________和________。
-
相关教案下载
- 12019-2020学年人教版必修2第1章第1节元素周期表第2课时学案
- 22019-2020学年人教版必修2第1章 第1节元素周期表第2课时学案
- 32019-2020学年人教版必修2第1章 第1节元素周期表第1课时学案
- 42018-2019学年人教版必修2 第1章第1节 元素周期表(第3课时) 学案
- 52018-2019学年人教版必修2 第1章第1节 元素周期表(第3课时) 学案(1)
- 62018-2019学年人教版必修2 第1章第1节 元素周期表(第1课时) 学案
- 72018-2019学年人教版必修2 第1章第1节 元素周期表(第2课时) 学案
- 82018-2019学年人教版必修2 第1章第1节 元素周期表(第1课时) 学案(1)
- 92018-2019学年人教版必修2 第1章第1节 元素周期表(第2课时) 学案(1)